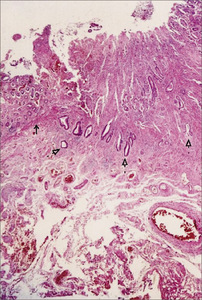
Naciekanie raka ograniczone do błony śluzowej określane jest literą m (mucosa) i zawiera trzy stopnie głębokości nacieku: m1– naciek dotyczący tylko nabłonka, m2 – naciek blaszki właściwej błony śluzowej, m3 – naciek blaszki mięśniowej błony śluzowej.
Podobnie na trzy stopnie podzielono naciek błony podśluzowej sm (submucosa): sm1 oznacza naciek obejmujący 1/3 grubości tej warstwy, sm2 – pomiędzy 1/3 a 2/3 błony podśluzowej i sm3 – ponad 2/3, ale bez nacieku warstwy mięśniowej właściwej (ryc. 5). Stopień sm1 można dodatkowo podzielić w zależności od rozległości poziomej nacieku na podstopnie: sm1a – gdy stosunek nacieku poziomego błony podśluzowej do powierzchownej wielkości zmiany wynosi mniej niż 1/4, sm1b – stosunek nacieku pomiędzy 1/4 a 1/2 i sm1c – ponad 1/2 (ryc. 6). Stopień nacieku błony podśluzowej jest niezmiernie istotny, gdyż według wielu wskazówek i wytycznych decyduje on o wyborze sposobu leczenia.[5]
Wraz ze wzrostem głębokości nacieku wzrasta też prawdopodobieństwo wystąpienia przerzutów do okolicznych węzłów chłonnych. Nie dysponujemy obecnie badaniem, które byłoby w stanie jednoznacznie wykluczyć ich obecność. Wskazane jest więc wykonanie podstawowych badań obrazowych, takich jak USG, KT czy EUS.
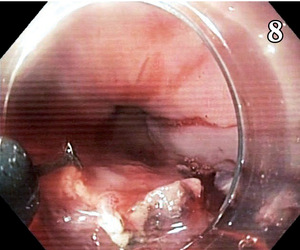
W latach 80. XX wieku w Japonii opracowano i upowszechniono nowoczesne techniki umożliwiające usunięcie wczesnych postaci raka techniką endoskopową. Techniki te, będące najmniej inwazyjnym postępowaniem, w wielu przypadkach okazały się radykalne i obecnie proponowane są jako metoda leczenia z wyboru. Podstawową techniką wprowadzoną w Japonii była endoskopowa mukozektomia – określana w piśmiennictwie terminem endoscopic mucosal resection (EMR).[6] Jest to metoda usuwania wycinków błony śluzowej i częściowo podśluzowej w jednym fragmencie. Zmiany po uprzednim ostrzyknięciu usuwa się pętlą elektryczną. W celu lepszego wyizolowania zmiany możliwe jest też zasysanie fragmentu błony śluzowej do wnętrza specjalnych nasadek zakładanych na endoskop lub zakładanie opasek gumowych na błonę śluzową przed jej usunięciem (ryc. 7). Drugą metodą, wprowadzoną później w celu poprawy radykalności resekcji, jest dyssekcja podśluzówkowa (ESD – endoscopic submucosal dissection). Po uprzednim wyznaczeniu granic resekcji i ostrzyknięciu zmiany błona śluzowa wraz z błoną podśluzową dookoła zmiany jest nacinana przy użyciu specjalnych noży elektrycznych (ryc. 8). Rodzaj wykorzystywanych narzędzi uzależniony jest od doświadczenia lekarza prowadzącego zabieg (ryc. 9). Technika ta pozwala na bardziej radykalne wycięcie zmiany, aż do błony mięśniowej właściwej (ryc. 10, 11).
Ostatecznie o leczeniu endoskopowym decyduje całkowite i swobodne uniesienie błony śluzowej wraz ze zmianą po jej ostrzyknięciu specjalnym roztworem (ryc. 12).
Techniki te zostały opracowane do usuwania wczesnych postaci raka. Można je stosować również do leczenia innych powierzchownych zmian patologicznych błony śluzowej, takich jak: gruczolaki, malformacje naczyniowe oraz guzków podśluzówkowych.[7] W naszym kraju pierwszy udokumentowany zabieg endoskopowego wycięcia wczesnego raka zgodnie ze standardami japońskimi wykonano w 2002 roku w Lublinie. Pacjentem był 78-letni mężczyzna z potwierdzonym rakiem gruczołowym wpustu żołądka. Zabieg wykonano w znieczuleniu ogólnym przy użyciu igły z ceramiczną końcówką (IT knife). Przebieg pooperacyjny bez powikłań. Chory podlegał regularnym badaniom kontrolnym i przeżył po zabiegu 10 lat.[8]
Korzystamy z doświadczeń japońskich
Od lat 80. XX wieku prowadzono głównie w Japonii badania kliniczne oparte na wielotysięcznych grupach chorych mające na celu sprecyzowanie wskazań do leczenia endoskopowego.[6, 9] Wskazania japońskie podlegają stałej aktualizacji, stanowią też wytyczną dla towarzystw naukowych w innych krajach.[5, 10, 11] Należy podkreślić, że obecnie prawie połowa nowotworów żołądka wykrywanych w Japonii to postaci wczesne. Również w naszym kraju korzystamy z tych doświadczeń. W grudniu 2012 roku w Lublinie podczas IX Międzynarodowego Sympozjum „Choroby Przełyku i Żołądka” doszło do spotkania, podczas którego ogłoszono aktualizację Polskiego Konsensusu Raka Żołądka – 2012.[12] Elementem tego konsensusu było endoskopowe leczenie wczesnych postaci raka żołądka. Poniżej przedstawiono podstawowe informacje obejmujące rozpoznanie, kwalifikację do leczenia, zasady przeprowadzenia zabiegu, pooperacyjną ocenę patologiczną i postępowanie po zabiegu.
Pamiętajmy jednak, że leczenie endoskopowe może mieć zastosowanie we wczesnym raku żołądka z niskim prawdopodobieństwem przerzutów do regionalnych węzłów chłonnych – Typ 0. Zmiany powinny kwalifikować się do usunięcia w jednym fragmencie.
Wskazania do leczenia endoskopowego
Istnieją dwa rodzaje wskazań do zabiegów endoskopowych: tzw. wskazania bezwzględne, które powinny być traktowane jako metoda leczenia z wyboru, oraz wskazania względne, rozszerzone, zarezerwowane do techniki dysekcji podśluzówkowej, które traktowane są jako postępowanie doświadczalne.
- Wskazania bezwzględne, standardowe: Typ wysoko zróżnicowany raka gruczołowego, bez cech owrzodzenia (UL-), gdzie głębokość naciekania nie przekracza błony śluzowej (T1a), a wymiar poprzeczny nie przekracza 2 cm.
- Wskazania względne, rozszerzone: Proponowaną techniką jest metoda dyssekcji podśluzówkowej. Wskazania rozszerzone proponowane są w guzach T1a z niskim prawdopodobieństwem przerzutów do węzłów chłonnych, spełniających poniższe kryteria:
- typ wysoko zróżnicowany raka bez cech owrzodzeń (UL-) o średnicy większej niż 2 cm
- typ wysoko zróżnicowany raka o charakterze owrzodziałym (UL+) o średnicy nieprzekraczającej 3 cm
- typ nisko zróżnicowany raka bez cech owrzodzeń (UL-) o średnicy nieprzekraczającej 2 cm.
Ocena skuteczności terapeutycznej
Obejmuje zarówno histopatologiczną ocenę usuniętego preparatu pod kątem radykalności, jak i prawdopodobieństwo wystąpienia przerzutów do węzłów chłonnych.