IV edycja Kongresu HPV już 12-13 czerwca! Poznaj najnowsze trendy w profilaktyce, diagnostyce i leczeniu raka szyjki macicy i innych schorzeń związanych z HPV | Sprawdź >
Kardiologia
Ablacja hybrydowa ze wsparciem lewokomorowym
Wojciech Skowroński
Konsultacja medyczna: dr Piotr Buchta
Zabiegów skomplikowanej ablacji hybrydowej ze wsparciem lewokomorowym u pacjentów z ciężką niewydolnością serca nie przeprowadzano do tej pory nawet w światowych ośrodkach. Powód? Zbyt duże ryzyko powikłań i śmierci chorego.
Jednak taki pacjent pozostawiony bez terapii i tak nie ma szans na przeżycie, dlaczego więc nie spróbować? – Zadaliśmy sobie to pytanie i zaryzykowaliśmy, szczególnie że byliśmy wyposażeni w bogate doświadczenie i niezawodny sprzęt – mówią lekarze ze Śląskiego Centrum Chorób Serca w Zabrzu.
– Niestabilny pod względem elektrycznym pacjent trafił do naszego ośrodka z powodu kilkudziesięciu groźnych napadów arytmii i wyładowań kardiowertera-defibrylatora. Mimo wielu prób nie potrafiliśmy go ustabilizować farmakologicznie – mówi dr n. med. Piotr Buchta z Oddziału Chorób Serca i Naczyń III Katedry i Oddziału Klinicznego Kardiologii SCCS w Zabrzu.
Pacjent z nietypową postacią ciężkiej niewydolności serca, prawdopodobnie z pozapalną etiologią, został najpierw poddany typowemu zabiegowi ablacji endokardialnej. Jednak serce w mapowaniu od wewnątrz wyglądało na zdrowe.
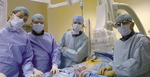
Ryc. 1. Zespół wykonujący zabieg, od lewej: dr n. med. Piotr Buchta (elektrofizjolog), dr n. med. Michał Hawranek (kardiolog interwencyjny), dr n. med. Michał Zembala i dr n. med. Krzysztof Filipiak (kardiochirurdzy).
– Każdorazowa indukcja arytmii w celu mapowania wiązała się ze znacznym spadkiem ciśnienia tętniczego, dlatego wszystkie nasze działania były podejmowane bardzo ostrożnie i w ograniczonym czasie. Najpierw wykonaliśmy więc wspomniany zabieg, ale po paru dniach częstoskurcz niestety powrócił. Zdawaliśmy sobie sprawę, że każde odstawienie dożylnych leków antyarytmicznych wywoła kolejną burzę elektryczną z kilkunastoma wyładowaniami z rzędu. W oparciu o wynik pierwszego badania elektrofizjologicznego i morfologię EKG częstoskurczu doszliśmy do wniosku, że jego źródło może znajdować się bardziej na zewnątrz. Powstał więc pomysł, by jednoczasowo kardiolodzy wykonali zabieg ablacji od wewnątrz, a kardiochirurdzy od zewnątrz. Do tego czasu utrzymywano leczenie farmakologiczne – dodaje dr Piotr Buchta (ryc. 1).
– Ponieważ częstoskurcz powodował spadki ciśnienia tętniczego nawet do poziomu 40 mmHg, wykonano ten zabieg przy użyciu specjalnego urządzenia do wspomagania lewej komory – małej pompki założonej na czas zabiegu do lewej komory serca z dostępu przezaortalnego. Gdy jego wydolność spadała, urządzenie zaczynało pracować i tłoczyć krew. Mimo niewielkich rozmiarów (6-7 cm) było w stanie wygenerować przepływ krwi od 3-5 litrów na minutę, czyli podobnie jak zdrowy narząd – tłumaczy dr n. med. Michał Hawranek, który wprowadzał pompkę w trakcie zabiegu.
Tego typu zabiegu opartego na wsparciu lewokomorowym w Polsce jeszcze nie wykonywano. Na świecie przeprowadzano analogiczne u chorych wysokiego ryzyka, ale bez podobnego zabezpieczenia i jednoczesnej ablacji elektrofizjologicznej – kardiologicznej i epikardialnej chirurgicznej. Ten skomplikowany zabieg, trwający blisko osiem godzin był wykonany przez kardiologów z dostępu przezskórnego przez żyły udowe, zaś kardiochirurgów – laparoskopowo. Dwa zespoły operujące korzystały jedynie z nakłuć i małych nacięć.
– Pacjent był przygotowywany podobnie jak do tradycyjnego zabiegu kardiochirurgicznego przeprowadzanego w znieczuleniu ogólnym, ale działaliśmy na „różnych piętrach” tego chorego. Najpierw zabezpieczyliśmy dostępy żylne dla naszych elektrod diagnostycznych i ablacyjnej, później kardiochirurdzy wykonali dostęp od strony otrzewnej dla torów wizyjnych i swojego narzędzia. Kolejny etap zabiegu to wykonanie dostępu do założenia specjalnej pompki. Została ona wprowadzona na długim prowadniku od strony tętnicy udowej, gwarantując małoinwazyjność, ale wymagając od chirurga precyzyjnego wypreparowania tej tętnicy – opisuje dr Buchta i dodaje: – Później wykonaliśmy nasz dostęp do lewej komory przez nakłucie transseptalne (przekłuwając przegrodę miedzyprzedsionkową), torując drogę elektrodzie ablacyjnej. Kolejny etap polegał na podłączeniu pompy i założeniu toru wizyjnego przez kardiochirurgów. Gdy wszystko poszło zgodnie z planem, zacząłem od środka mapować komorę, aby potwierdzić przeprowadzone badania obrazowe i w końcu znaleźć źródło częstoskurczu. Po aplikacjach od wewnątrz serca, we wskazanym miejscu kardiochirurdzy wykonali aplikacje od zewnątrz, pod kontrolą wzroku. Stanowi to pewną nowość, gdyż przeprowadzane epikardialnie ablacje od strony elektrofizjologicznej opierają się na systemie tworzącym trójwymiarową mapę wirtualną, a w tym przypadku operujący dokładnie widzą, oceniają wygląd tkanki i jej przyleganie do elektrody.
Przypadek pacjenta, u którego wykonano ten zabieg, był nietypowy.
– Są takie miejsca w sercu, które mają grubą mięśniówkę i użycie źródła, czy tylko z zewnątrz, czy z wewnątrz, nie gwarantuje pozytywnego skutku. Jeśli zmiana zlokalizowana jest głęboko, to energia aplikacji może nie dotrzeć na odpowiednią odległość (nie ma takiej możliwości penetracji), ale połączone siły z jednej i drugiej strony dały bardzo dobry efekt – komentuje dr Buchta.
Pacjent po zabiegu czuje się dobrze i co najważniejsze, nie pojawiają się u niego żadne zaburzenia rytmu.
– Najtrudniejszym momentem było znalezienie miejsca odpowiedzialnego za zaburzenia rytmu. Nie wiedzieliśmy, czy będziemy mogli je poprawnie zidentyfikować. Druga wątpliwość to oczywiście stan pacjenta obciążonego niską frakcją wyrzutową – mówi dr n. med. Michał Zembala, kardiochirurg z SCCS.
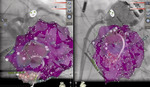
Ryc. 2. Mapa potencjałowa Carto Univu lewej komory z miejscem aplikacji i obrazem naczyń wieńcowych. Widoczne elektrody diagnostyczne, ablacyjna oraz pompa Impella. Projekcja RAO (strona lewa) i LAO (strona prawa).
Zabieg mimo wielu wątpliwości i zagrożeń przebiegał zgodnie z planem (ryc. 2-3).
– Zarówno jego strategia, jak i precyzyjne wykonanie wpłynęły na bezpieczny przebieg. Oczywiście obawiamy się jeszcze powikłań w postaci wystąpienia zaburzeń rytmu serca pochodzących z tego ogniska, ale na razie objawy ustąpiły i to nas bardzo cieszy – komentuje dr Michał Zembala i podkreśla małoinwazyjność zabiegu, która przyczyniła się z pewnością do takich efektów.
– Już wiele lat temu próbowano leczenia hybrydowego, elektrofizjologicznego, kardiochirurgicznego, ale tym razem udało nam się wykonać zabieg z dostępów całkowicie nieinwazyjnych. Zarówno część kardiochirurgiczna, wykonana endoskopowo przy użyciu kamery, jak i część kardiologiczna przebiegały przy skrajnie niskiej inwazyjności – podsumowuje dr Zembala.
Do tej pory w SCCS w Zabrzu zabiegi ablacji hybrydowej były wykorzystywane głównie w przypadku migotania przedsionków. To jednak z anatomicznego punktu widzenia działanie łatwiejsze. W przypadku opisywanego zabiegu ułatwieniem z pewnością był sprzęt, z którego mogli skorzystać zabrzańscy lekarze. Oprócz pompki (wykorzystywanej do tej pory tylko w czasie zabiegów angioplastyki wieńcowej wysokiego ryzyka) korzystali z nowoczesnego oprogramowania, które przy użyciu lampy rentgenowskiej ułatwiło nałożenie wirtualnej mapy na trójwymiarową mapę serca i zlokalizowanie miejsca arytmii. Co najważniejsze – w trakcie rehabilitacji wewnątrzszpitalnej, aż do wypisu, nie nawróciły żadne zaburzenia rytmu i chory mógł bezpiecznie opuścić szpital.