IV edycja Kongresu HPV już 12-13 czerwca! Poznaj najnowsze trendy w profilaktyce, diagnostyce i leczeniu raka szyjki macicy i innych schorzeń związanych z HPV | Sprawdź >
Ortopedia
Przeszczepienie chondrocytów alternatywą dla endoprotezy
Alicja Giedroyć
Konsultacja medyczna: prof. Szymon Dragan
W Uniwersyteckim Szpitalu Klinicznym we Wrocławiu rozpoczęły się przygotowania do przeszczepiania komórek własnej chrząstki pacjentów ze zmianami zwyrodnieniowymi kolan. Wcześniej w Klinice Ortopedii i Traumatologii Narządów Ruchu USK wykonywano już takie zabiegi u kilkunastu pacjentów, ale obecnie przygotowywane jest opracowanie własnej technologii hodowli chondrocytów, a plany sięgają znacznie dalej niż tylko odtwarzanie tkanki chrzęstnej przy niewielkich ubytkach. Ostatecznym celem rozpoczętego projektu badawczego jest odtworzenie całego stawu.
– Biologiczna regeneracja tkanek poprzez odtworzenie własnej chrząstki i przywrócenie prawidłowej powierzchni stawów komórek to dla wielu pacjentów szansa na uniknięcie w przyszłości endoprotezy – tłumaczy prof. dr hab. med. Szymon Dragan, kierownik Kliniki Ortopedii i Traumatologii Narządów Ruchu USK. – Usunięcie stawu i wstawienie w jego miejsce protezy, które stosuje się przy dużych zmianach zwyrodnieniowych, jest drastycznym zabiegiem, zagrożonym powikłaniami zarówno pooperacyjnymi, jak i śródoperacyjnymi. Jednocześnie są to zabiegi powszechne – rocznie na świecie wykonuje się kilkanaście milionów takich operacji. Zwyrodnienia są bowiem ogromnym problemem społecznym, który w dodatku wciąż narasta, w związku ze starzeniem się społeczeństw, a także nieprawidłowym trybem życia. Poszukiwanie alternatywnych, bezpieczniejszych dla pacjenta metod to tym bardziej ważne wyzwanie. Ochrona i leczenie chrząstki, zanim dojdzie do zaawansowanego IV stopnia zwyrodnienia, jest obiecującym kierunkiem.
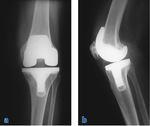
Osoby ze zmianami zwyrodnieniowymi stawów (głównie w zakresie stawu kolanowego i biodrowego) stanowią jedną z największych grup pacjentów kliniki. Jej szef zwraca uwagę, że coraz więcej pacjentów to ludzie młodzi, zwykle uprawiający sporty ekstremalne, u których do zwyrodnień doszło na skutek urazów. Nadal jednak większość to osoby powyżej 60. r.ż., a więc w wieku, w którym najczęściej dochodzi do rozwoju artrozy. W początkowej jej fazie leczenie polega na stymulowaniu wzrostu tkanki chrzęstnej poprzez stosowanie fizykoterapii oraz podawanie (doustnie lub poprzez wstrzykiwanie do stawu) preparatów wzmacniających chrząstkę lub aktywujących w niej procesy naprawy. Na przykład do stawu wprowadza się preparaty zawierające składniki chrząstki stawowej, takie jak siarczan chondroityny i kolagen, osocze bogatopłytkowe zawierające czynniki wzrostu, hialuronian sodu, tzw. kwas hialuronowy, czy komórki macierzyste. W IV stopniu zwyrodnień, gdy dochodzi już do odsłonięcia kości, która w dużej części przestaje być pokryta tkanką chrzęstną, takie działania są już niewystarczające i pozostaje chirurgiczne „wycięcie” stawu oraz zastąpienie go wszczepioną endoprotezą (ryc. 1). Z piśmiennictwa światowego wynika, że w 2005 roku wszczepiono na świecie 532 tys. endoprotez kolana, a szacowany jest blisko siedmiokrotny wzrost liczby tych operacji w 2030 roku do 3 mln 480 tys.
– Ratowanie chrząstki ma największy sens w zwyrodnieniach I i II stopnia, gdy staje się ona rozmiękła, a ubytki są niewielkie – mówi prof. Szymon Dragan. – III stopień, kiedy chrząstka odrywa się już od podłoża kostnego, to etap graniczny.
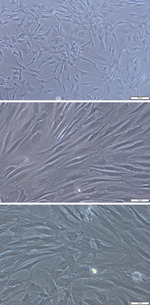
Jedną z metod biologicznej regeneracji zniszczonych stawów jest wszczepienie produkujących kolagen chondrocytów, namnożonych w laboratorium z pobranej wcześniej tkanki chrzęstnej pacjenta. Jednak przy dzisiejszych technologiach w ten sposób można próbować odtwarzać tkankę chrzęstną tylko przy niewielkich ubytkach – implant służący do wypełnienia ubytku zwykle jest wielkości do 2 × 2 cm (ryc. 2).
– Ponadto metoda nie zawsze jest skuteczna – zastrzega prof. Dragan. – Często chondrocyty świetnie się namnażają in vitro, ale wprowadzone do organizmu tracą tę zdolność. Wadą jest także to, że chondrocyty w obecnie stosowanych technologiach namnażają się jednowarstwowo, tworząc płaskie struktury. Ich właściwości regeneracyjne byłyby znacznie lepsze, gdyby udało się stworzyć strukturę przestrzenną.
I to właśnie jest jednym z celów Pracowni Eksperymentalnej Komórkowej Regeneracji Tkanek wrocławskiego USK, stworzonej na początku tego roku m.in. w celu opracowania własnej metodologii hodowli chondrocytów. Powstanie i wyposażenie takiego laboratorium to ogromne koszty, przewyższające na ogół możliwości polskich ośrodków medycznych. We Wrocławiu udało się to dzięki wsparciu Fundacji Uniwersytetu Medycznego, a także wspierających rozwój nauki poprzez własne fundacje przedstawicieli przemysłu – Kombinatu Górniczo-Hutniczego Miedzi i Tauron Polska.
Pracownią kieruje prof. dr hab. med. Julia Bar, kierownik Zakładu Immunopatologii i Biologii Molekularnej w Katedrze Patomorfologii i Cytologii Onkologicznej.
Eksperymenty rozpoczęły się od materiału pobranego z tkanki chrzęstnej stawu kolanowego.
– Pobrany z kolana fragment chrząstki jest w laboratorium cięty i poddany obróbce enzymatycznej – tłumaczy prof. Julia Bar. – Odpowiednio dobrane enzymy muszą strawić tkankę, by można z niej było wyizolować ok. 800 tys. chondrocytów. Materiał bywa różnorodny, u jednych pacjentów komórek jest więcej, u innych mniej. Bardzo zróżnicowana jest także ich aktywność, a różnice są zauważalne nawet w obrębie tego samego stawu, bo degeneracja tkanek jest nierównomierna.
Celem hodowli chondrocytów jest zwiększenie ich liczebności do kilku milionów. W warunkach laboratoryjnych hodowla trwa około sześciu tygodni. W tym czasie na bieżąco sprawdza się aktywność proliferacyjną chondrocytów oraz to, czy wykazują właściwy fenotyp, czyli zdolność do produkcji kolagenu.
Wyniki pierwszych eksperymentów we wrocławskiej pracowni prof. Julia Bar ocenia jako obiecujące: – Udało się nam przywrócić funkcje biologiczne wcześniej przechowywanych chondrocytów w głębokim zamrożeniu (-86°C). W przyszłości może mieć to kolosalne znaczenie i rozwiązać problemy związane z koniecznością powtórzenia zabiegu u pacjenta.
Jeszcze większe znaczenie może mieć uzyskanie hodowli chondrocytów w strukturze 3D. Pierwsze rezultaty już są – komórki umieszczone na specjalnym podłożu, które jest rodzajem rusztowania, zaczynają się namnażać. Prof. Bar, choć jest zadowolona ze wstępnych efektów, zastrzega, że na ostateczne wyniki trzeba jeszcze poczekać przynajmniej kilka tygodni, a potem powtarzać eksperyment.
– Pierwsze udane eksperymenty z tkanką chrzęstną stanowią zachętę do rozszerzenia prac nad hodowlą komórek, które mogą być wykorzystane w chorobach neurodegeneracyjnych, ale także np. w okulistyce – dodaje prof. Bar. – Pracujemy także m.in. nad stworzeniem własnej metody stymulacji produkcji kolagenu przez chondrocyty. W tym celu chcemy zastosować endogenne czynniki wzrostu.
Prof. Dragan ocenia, że już pod koniec tego roku we wrocławskim ośrodku na bazie chondrocytów powstaną preparaty, które będą mogły być substytutem chrząstki stawowej. A to tylko pierwszy krok do bardziej ambitnego celu, jakim jest opracowanie własnej technologii odtworzenia całego stawu.